Кислота – молекула или ион, способные отдавать протон. Каждой кислоте соответствует сопряженное с нею основание. Сила кислот характеризуется константой кислоты Кк.
Н2CO3 + Н2O ↔ Н3O+ + HCO3¯
Кк = 4 × 10-7
[Al(Н2O)6]3+ + Н2O ↔ [Al(Н2O)5OH]2+ + Н3O+
Кк = 9 × 10-6
Основание – молекула или ион, способные принимать протон. Каждому основанию соответствует сопряженная с ним кислота. Сила оснований характеризуется константой основания К0.
NH3 × Н2O (Н2O) ↔ NH4+ + OH¯
К0= 1,8 ×10-5
Амфолиты – протолиты, способные к отдаче и к присоединению протона.
HCO3¯ + H2O ↔ Н3O+ + CO32-
HCO3¯ – кислота.
HCO3¯ + H2O ↔ Н2CO3 + OH¯
HCO3¯ – основание.
Для воды: Н2O+ Н2O ↔ Н3O+ + OH¯
K(H2O) = [Н3O+][OH¯] = 10-14 и рН = – lg[H3O+].
Константы Кк и К0 для сопряженных кислот и оснований связаны между собой.
НА + Н2O ↔ Н3O+ + А¯,
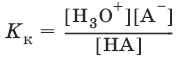
А¯ + Н2O ↔ НА + OH¯,
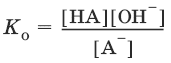
Отсюда
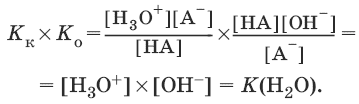
7. Константа растворимости. Растворимость
В системе, состоящей из раствора и осадка, идут два процесса – растворение осадка и осаждение. Равенство скоростей этих двух процессов является условием равновесия.
Насыщенный раствор – раствор, который находится в равновесии с осадком.
Закон действия масс в применении к равновесию между осадком и раствором дает:
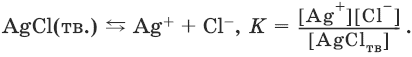
Поскольку [AgClтв] = const,
К • [AgClтв] = Ks(AgCl) = [Ag+] • [Cl¯].
В общем виде имеем:
АmBn(тв.) ↔ mA+n + nB-m
Ks(AmBn) = [А+n]m • [В-m]n.
Константа растворимости Ks (или произведение растворимости ПР) – произведение концентраций ионов в насыщенном растворе малорастворимого электролита – есть величина постоянная и зависит лишь от температуры.
Растворимость малорастворимого вещества s может быть выражена в молях на литр. В зависимости от величины s вещества могут быть разделены на малорастворимые – s < 10-4 моль/л, среднерастворимые – 10-4 моль/л ≤ s ≤ 10-2 моль/л и хорошо растворимые s >10-2 моль/л.
Растворимость соединений связана с их произведением растворимости.
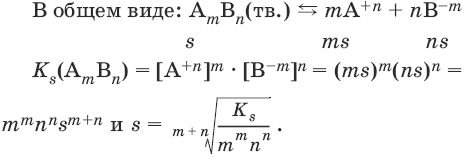
В случае AgCl: AgCl ↔ Ag+ + Cl¯
Ks = [Ag+] • [CI¯]:
а) условие равновесия между осадком и раствором: [Ag+] • [Cl¯] = Ks.
б) условие осаждения: [Ag+] • [Cl¯] > Ks; в ходе осаждения концентрации ионов уменьшаются до установления равновесия;
в) условие растворения осадка или существования насыщенного раствора: [Ag+] • [Cl¯] < Ks; в ходе растворения осадка концентрация ионов увеличивается до установления равновесия.
8. Координационные соединения
Координационные (комплексные) соединения – соединения с донорно-акцеп-торной связью.
Для K3[Fe(CN)6]:
ионы внешней сферы – 3К+,
ион внутренней сферы – [Fe(CN)6]3-,
комплексообразователь – Fe3+,
лиганды – 6CN¯, их дентатность – 1,
координационное число – 6.
Примеры комплексообразователей: Ag+, Cu2+, Hg2+, Zn2+, Ni2+, Fe3+, Pt4+ и др.
Примеры лигандов: полярные молекулы Н2O, NH3, CO и анионы CN¯, Cl¯, OH¯ и др.
Координационные числа: обычно 4 или 6, реже 2, 3 и др.
Номенклатура. Называют сначала анион (в именительном падеже), затем катион (в родительном падеже). Названия некоторых лигандов: NH3 – аммин, Н2O – акво, CN¯ – циано, Cl¯ – хлоро, OH¯ – гидроксо. Названия координационных чисел: 2 – ди, 3 – три, 4 – тетра, 5 – пента, 6 – гекса. Указывают степень окисления комплек-сообразователя:
[Ag(NH3)2]Cl – хлорид диамминсеребра(I);
[Cu(NH3)4]SO4 – сульфат тетрамминмеди(II);
K3[Fe(CN)6] – гексацианоферрат(III) калия.
Теория валентных связей предполагает гибридизацию орбиталей центрального атома. Расположение образующихся при этом гибридных орбиталей определяет геометрию комплексов.
Диамагнитный комплексный ион Fe(CN)64-.
Цианид-ион – донор
Ион железа Fe2+ – акцептор – имеет формулу 3d64s04p0. С учетом диамагнитности комплекса (все электроны спарены) и координационного числа (нужны 6 свободных орбиталей) имеем d2sp3-гибридизацию:
Комплекс диамагнитный, низкоспиновый, внутриорбитальный, стабильный (не используются внешние электроны), октаэд-рический (d2sp3-гибридизация).
Парамагнитный комплексный ион FeF63-.
Фторид-ион – донор.
Ион железа Fe3+ – акцептор – имеет формулу 3d54s04p0. С учетом парамагнитности комплекса (электроны распарены) и координационного числа (нужны 6 свободных орбиталей) имеем sp3d2-гибридизацию:
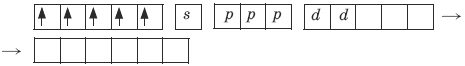
Комплекс парамагнитный, высокоспиновый, внешнеорбитальный, нестабильный (использованы внешние 4d-орбитали), октаэдрический (sp3d2-гибридизация).
Координационные соединения в растворе полностью диссоциируют на ионы внутренней и внешней сфер.
[Ag(NH3)2]NO3 → Ag(NH3)2+ + NO3¯, α = 1.
Ионы внутренней сферы, т. е. комплексные ионы, диссоциируют на ионы металла и лиганды, как слабые электролиты, по ступеням.

где K1, К2, К1_2 называются константами нестойкости и характеризуют диссоциацию комплексов: чем меньше константа нестойкости, тем меньше диссоциирует комплекс, тем он устойчивее.
II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
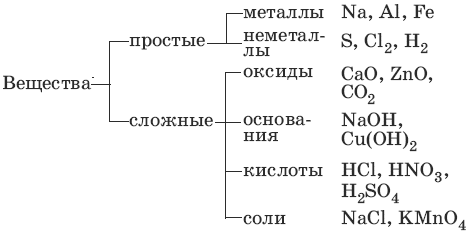
1. Основные классы неорганических соединений